Gli scienziati svelano il meccanismo alla base della produzione di ammoniaca più ecologica
Annunci
I ricercatori della Tokyo Metropolitan University hanno rivelato come un catalizzatore di una promettente reazione chimica per l'industria contribuisca alla produzione di ammoniaca, uno dei principali ingredienti dei fertilizzanti. L'ossido di rame è un catalizzatore chiave nella reazione elettrochimica di riduzione dei nitrati, un'alternativa più ecologica all'attuale processo Haber-Bosch. I ricercatori hanno scoperto che le particelle di rame si creano a metà della reazione, aiutando a convertire gli ioni nitrito in ammoniaca. Questa conoscenza dei meccanismi sottostanti promette passi da gigante nello sviluppo di una nuova chimica industriale.
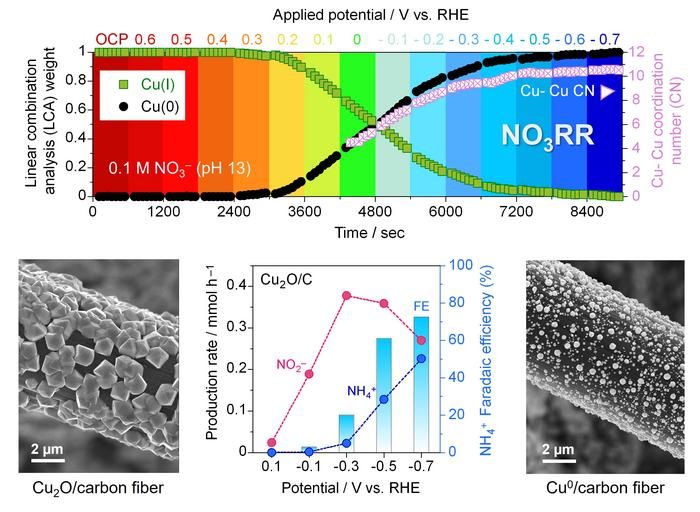
(in alto) Proporzione di rame (I) nell'ossido di rame e di rame (0) nelle particelle di rame metallico sotto diverse tensioni applicate. Una tensione più negativa è correlata alla comparsa di un maggior numero di legami Cu-Cu. (in basso a sinistra) Immagine al microscopio elettronico a scansione (SEM) di particelle di ossido di rame montate su fibra di carbonio. (in basso a destra) Tasso di produzione di ioni nitrito e ammonio a diverse tensioni ed efficienza della produzione di ammonio. (in basso a destra) Immagine al SEM di particelle di rame metallico su fibra di carbonio.
Tokyo Metropolitan University
Come ingrediente dei fertilizzanti, l'ammoniaca è una sostanza chimica importante per l'agricoltura industriale. Il metodo più diffuso per produrre ammoniaca è il processo Haber-Bosch, in cui azoto e idrogeno vengono fatti reagire ad alta temperatura e pressione. Questo processo è ad alta intensità energetica e si ritiene che sia responsabile di circa l'1,4% delle emissioni globali di anidride carbonica. Essendo una sostanza chimica alla base di gran parte della produzione alimentare, è in corso la caccia a metodi più ecologici per produrre ammoniaca.
Un team guidato dal professor Fumiaki Amano della Tokyo Metropolitan University ha studiato la reazione elettrochimica di riduzione dei nitrati, un'alternativa promettente che può produrre ammoniaca dai nitrati a temperatura e pressione ambiente. I processi elettrochimici funzionano inserendo degli elettrodi in una miscela chimica e applicando una tensione per pilotare le reazioni. Nonostante i numerosi studi che hanno identificato le reazioni specifiche che avvengono agli elettrodi durante la produzione di ammoniaca, il meccanismo esatto si è rivelato sfuggente.
Utilizzando tecniche all'avanguardia, il team ha ottenuto una visione senza precedenti di come l'ammoniaca viene prodotta in presenza di un catalizzatore di ossido di rame, uno degli elettrocatalizzatori più efficaci per questo tipo di reazione. Hanno utilizzato l'assorbimento operando dei raggi X, un metodo che combina la comprensione degli stati elettronici con la conoscenza dei legami e della struttura locale. Montando piccole particelle di ossido di rame su fibre di carbonio, sono riusciti a capire come cambiano le cose quando la tensione viene resa più negativa durante la reazione. In presenza di una tensione positiva, è stato dimostrato che gli ioni nitrato "passivano" il catalizzatore assorbendo su di essi e impedendo la conversione dell'ossido di rame in rame metallico, producendo invece ioni nitrito. Quando la tensione diventa più negativa, la produzione di ammoniaca aumenta bruscamente. Ciò avviene in concomitanza con la comparsa di particelle di rame metallico, evidenziata da un drastico aumento del numero di legami rame-rame. Hanno scoperto che il rame metallico contribuisce ad aggiungere idrogeno agli ioni nitrito per produrre ammoniaca.
Le misurazioni del team hanno mostrato come la passivazione della superficie influisca sull'efficienza del catalizzatore di ossido di rame e come la produzione di rame metallico sia fondamentale per la produzione efficiente di ammoniaca. Il loro lavoro evidenzia un'ampia classe di strategie per ottimizzare la produzione di ammoniaca verde e progettare nuovi catalizzatori elettrochimici.
Questo lavoro è stato sostenuto dalla Tokyo Metropolitan University e dal Tokyo Global Partner Scholarship Program e si basa sui risultati ottenuti dal progetto JPNP14004 commissionato dalla New Energy and Industrial Technology Development Organization (NEDO).
Nota: questo articolo è stato tradotto utilizzando un sistema informatico senza intervento umano. LUMITOS offre queste traduzioni automatiche per presentare una gamma più ampia di notizie attuali. Poiché questo articolo è stato tradotto con traduzione automatica, è possibile che contenga errori di vocabolario, sintassi o grammatica. L'articolo originale in Inglese può essere trovato qui.









































