Des scientifiques dévoilent le mécanisme à l'origine d'une production d'ammoniac plus écologique
Annonces
Des chercheurs de l'université métropolitaine de Tokyo ont révélé comment un catalyseur d'une réaction chimique prometteuse pour l'industrie contribue à la production d'ammoniac, un ingrédient majeur des engrais. L'oxyde de cuivre est un catalyseur clé dans la réaction électrochimique de réduction des nitrates, une alternative plus écologique au procédé Haber-Bosch existant. Les chercheurs ont découvert que des particules de cuivre sont créées au milieu de la réaction, aidant à convertir les ions nitrite en ammoniac. Cette compréhension des mécanismes sous-jacents promet des avancées dans le développement d'une nouvelle chimie industrielle.
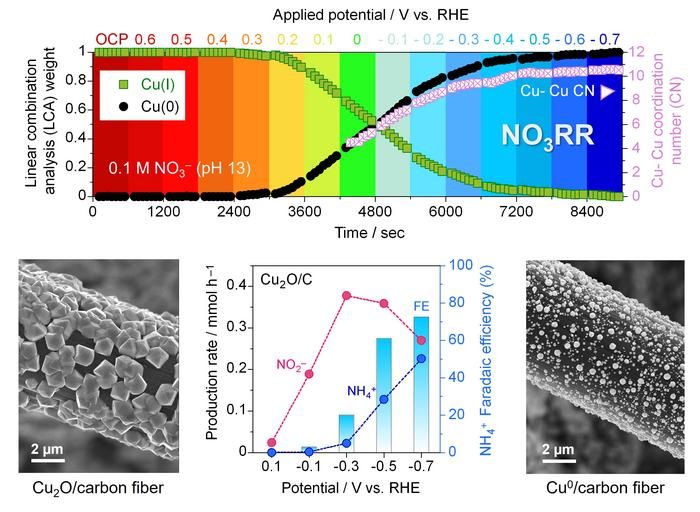
(en haut) Proportion de cuivre (I) dans l'oxyde de cuivre et de cuivre (0) dans les particules de cuivre métallique sous différentes tensions appliquées. Une tension plus négative correspond à l'apparition d'un plus grand nombre de liaisons Cu-Cu. (en bas à gauche) Image de microscopie électronique à balayage (MEB) de particules d'oxyde de cuivre montées sur de la fibre de carbone. (en bas à gauche) Taux de production d'ions nitrite et ammonium à différentes tensions, et efficacité de la production d'ammonium. (en bas à droite) Image au microscope électronique à balayage (MEB) de particules métalliques de cuivre montées sur une fibre de carbone.
Tokyo Metropolitan University
En tant qu'ingrédient des engrais, l'ammoniac est un produit chimique important pour l'agriculture industrielle. La méthode la plus répandue pour produire de l'ammoniac est le procédé Haber-Bosch, qui consiste à faire réagir l'azote et l'hydrogène à une température et une pression élevées. Ce procédé est donc très énergivore ; il représenterait environ 1,4 % des émissions mondiales de dioxyde de carbone. Ce produit chimique étant à la base d'une grande partie de la production alimentaire, la recherche de méthodes plus écologiques de fabrication de l'ammoniac est en cours.
Une équipe dirigée par le professeur Fumiaki Amano de l'université métropolitaine de Tokyo a étudié la réaction électrochimique de réduction des nitrates, une alternative prometteuse qui permet de produire de l'ammoniac à partir de nitrates à température et pression ambiantes. Les processus électrochimiques consistent à placer des électrodes dans un mélange chimique et à appliquer une tension pour déclencher des réactions. Malgré de nombreuses études identifiant des réactions spécifiques se produisant au niveau des électrodes lors de la production d'ammoniac, le mécanisme exact s'est avéré difficile à cerner.
En utilisant des techniques de pointe, l'équipe a obtenu des informations sans précédent sur la façon dont l'ammoniac est produit en présence d'un catalyseur à base d'oxyde de cuivre, l'un des électrocatalyseurs les plus efficaces pour ce type de réaction. Ils ont utilisé l'absorption de rayons X operando, une méthode combinant la compréhension des états électroniques et la connaissance de la liaison et de la structure locales. En montant de petites particules d'oxyde de cuivre sur des fibres de carbone, ils ont réussi à extraire la manière dont les choses changent lorsque la tension est rendue plus négative au cours de la réaction. Sous une tension positive, il a été démontré que les ions nitrate "passivaient" le catalyseur en absorbant sur eux et en empêchant la conversion de l'oxyde de cuivre en cuivre métallique, en produisant des ions nitrite à la place. Lorsque la tension devient plus négative, la production d'ammoniac augmente brusquement. Cela se produit en même temps que l'apparition de particules de cuivre métallique, mise en évidence par une augmentation spectaculaire du nombre de liaisons cuivre-cuivre. Les chercheurs ont découvert que le cuivre métallique contribue à ajouter de l'hydrogène aux ions nitrite pour produire de l'ammoniac.
Les mesures de l'équipe ont montré comment la passivation de la surface affecte l'efficacité du catalyseur à base d'oxyde de cuivre et comment la production de cuivre métallique est cruciale pour la production efficace d'ammoniac. Leurs travaux mettent en évidence une vaste catégorie de stratégies visant à optimiser la production d'ammoniac vert et à concevoir de nouveaux catalyseurs électrochimiques.
Ce travail a été soutenu par la Tokyo Metropolitan University et le Tokyo Global Partner Scholarship Program et s'appuie sur les résultats obtenus dans le cadre du projet JPNP14004 commandé par la New Energy and Industrial Technology Development Organization (NEDO).
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Annonces















































