Rivelato il meccanismo di roaming nel bromoformio
L'esperimento fornisce la prova del meccanismo di roaming nelle reazioni fotochimiche, a lungo dibattuto
Annunci
Il composto alometano bromoformio (CHBr3) ha effetti devastanti sullo strato di ozono. Negli strati superiori dell'atmosfera, il bromoformio reagisce con i raggi UV, rilasciando molecole di bromo che distruggono le molecole di ozono. Questa reazione, tuttavia, ha lasciato a lungo perplessi gli scienziati: le molecole coinvolte sembrano vagare l'una rispetto all'altra in un modo che energeticamente non ha senso. Gli scienziati dell'European XFEL hanno ora rivelato per la prima volta le prove strutturali di questo meccanismo di vagabondaggio, stabilendo che si tratta di una caratteristica universale delle reazioni fotochimiche. Lo studio, pubblicato su Nature Communications, fornisce indicazioni fondamentali per il campo della fotochimica atmosferica e per il modo in cui i composti alometanici come il bromoformio influiscono sullo strato di ozono.
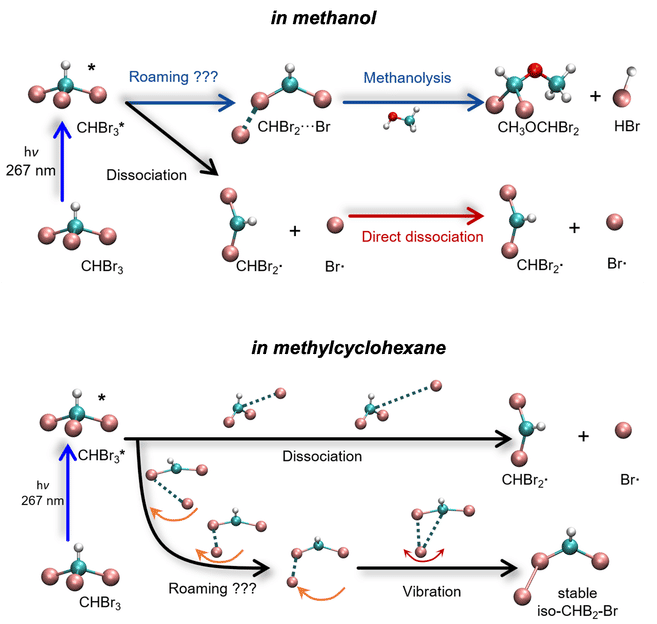
Didascalia: Dinamica di reazione appena chiarita del bromoformio (CHBrâ'ƒ) nei solventi metanolo (in alto) e metilcicloesano (in basso). Gli atomi sono rappresentati come segue: carbonio (ciano), bromo (rosa), idrogeno (grigio) e ossigeno (rosso).
European XFEL
Lo strato di ozono avvolge la Terra a circa 15-30 km sopra la superficie del pianeta. Il gas ozono assorbe la luce ultravioletta quando entra nell'atmosfera, proteggendo così la vita sulla Terra dagli effetti delle radiazioni nocive. L'ozono, tuttavia, reagisce facilmente con altri composti che si trovano nella stratosfera, portando alla riduzione dell'ozono e, in ultima analisi, alla creazione del buco dell'ozono. Uno di questi composti è il bromoformio (CHBr3). Emesso dalla vita marina, come il fitoplancton e le alghe, questo composto alometano interagisce con la luce UV quando si sposta negli strati superiori dell'atmosfera, sospeso in gocce d'acqua o aerosol. L'interazione con la luce UV innesca una reazione che porta al rilascio di molecole di bromo. Più di 100 volte più distruttivo di altri gas alogeni come il cloro, il bromo è estremamente reattivo e distrugge rapidamente le molecole di ozono. Questo tipo di fotoreazioni è all'origine del buco dell'ozono. Ora, utilizzando l'XFEL europeo, gli scienziati hanno rivelato dettagli strutturali chiave di questo tipo di reazione, migliorando la nostra comprensione della chimica atmosferica.
L'enigma delle molecole vaganti
I dettagli della reazione ultraveloce indotta dalla luce che coinvolge il bromoformio hanno lasciato a lungo perplessi gli scienziati. È noto che dopo l'interazione iniziale con la luce UV, il bromoformio si rompe in frammenti, alcuni dei quali si riallineano per formare composti chimici stabili. Tuttavia, curiosamente, le molecole coinvolte in queste reazioni non si comportano come ci si aspetterebbe. "Alla fine si formano complessi intermedi stabili dopo che il bromoformio viene frammentato dalla luce UV", spiega Qingyu Kong, scienziato del sincrotrone Soleil e principale collaboratore dello studio. "Tuttavia, nelle fasi iniziali della reazione questi frammenti possono unirsi in configurazioni strutturali che non sembrano avere senso dal punto di vista energetico, almeno nella visione classica. Piuttosto che separarsi completamente o legarsi in un modo che richiede la minor quantità di energia, i frammenti migrano lentamente l'uno rispetto all'altro in un modo che aggira gli stati di transizione convenzionali". Per spiegare queste osservazioni, gli scienziati hanno formulato l'ipotesi del roaming, che indica il modo in cui gli ioni sembrano allontanarsi per trovare una nuova configurazione stabile. Tuttavia, finora non è stata fornita alcuna prova strutturale diretta a sostegno di questa teoria nel bromoformio.
Utilizzando l'XFEL europeo, un team di ricercatori ha risolto per la prima volta questo meccanismo di roaming ultraveloce. Studi precedenti condotti su sincrotroni hanno rivelato i prodotti finali di queste reazioni, ma non sono stati in grado di svelare le fasi iniziali. "Era evidente che la prima fase cruciale della reazione, in cui si pensa avvenga il meccanismo di roaming, avviene molto più velocemente di quanto gli impulsi di raggi X del sincrotrone potessero rilevare", spiega Dmitry Khakhulin, scienziato europeo dell'XFEL e autore principale del recente studio.
Impulsi di femtosecondi fanno il trucco
Per il loro esperimento, gli scienziati hanno iniettato soluzioni di bromoformio sotto forma di getti sottili nell'area dell'esperimento presso lo strumento FXE dell'European XFEL. Un impulso laser ottico a femtosecondi ha innescato la reazione; un impulso a raggi X ritardato è stato poi utilizzato per acquisire informazioni sulle diverse fasi della reazione. Il metodo è noto come scattering di soluzioni a raggi X risolto in tempo di femtosecondi.
A differenza degli esperimenti precedenti, gli impulsi di raggi X ultracorti generati dall'XFEL europeo hanno permesso agli scienziati di catturare tutte le fasi strutturali della reazione, dalla rottura dei primi legami e dalle dinamiche di vagabondaggio dei frammenti alla formazione di bromo e di vari prodotti di ricombinazione. I risultati hanno mostrato che entro 150 femtosecondi dall'inizio della reazione, il roaming ha avuto luogo e i composti intermedi stabili hanno iniziato a formarsi gradualmente.
"Grazie agli impulsi di raggi X ultracorti generati dall'XFEL europeo, siamo stati in grado di fornire per la prima volta la prova strutturale del roaming nel bromoformio", spiega Khakhulin.
Influenza del solvente
Studi precedenti condotti su sincrotroni indicavano anche che l'esito della reazione era influenzato dal solvente. Per i loro studi all'European XFEL, gli scienziati hanno utilizzato due liquidi diversi come solventi - metanolo e metilcicloesano - per determinare se questo fosse il caso.
"I nostri risultati hanno mostrato che, sebbene l'intermedio si formasse in entrambi i liquidi, ciò che accadeva dopo dipendeva fortemente dal solvente in cui era sospeso il bromoformio", spiega Kong. Quando era sospeso in metanolo, le molecole di metanolo competevano per legarsi al composto intermedio e quindi l'intermedio iniziale a vita breve si decomponeva. Il metilcicloesano, invece, meno reattivo, ha fatto sì che l'intermedio si rilassasse in un prodotto stabile.
"Nel complesso, queste nuove conoscenze rappresentano un passo importante verso una comprensione più completa della fotochimica atmosferica e offrono un nuovo quadro per comprendere il comportamento di composti come il bromoformio nel contesto dell'ambiente in fase gassosa, degli aerosol e delle gocce d'acqua", conclude Kong.
Questo studio è stato condotto nell'ambito di una collaborazione a lungo termine presso lo strumento FXE. Il lavoro ha richiesto una stretta collaborazione tra l'XFEL europeo, il sincrotrone Soleil, l'Università di ShanghaiTech e l'ESRF.
Nota: questo articolo è stato tradotto utilizzando un sistema informatico senza intervento umano. LUMITOS offre queste traduzioni automatiche per presentare una gamma più ampia di notizie attuali. Poiché questo articolo è stato tradotto con traduzione automatica, è possibile che contenga errori di vocabolario, sintassi o grammatica. L'articolo originale in Inglese può essere trovato qui.
Pubblicazione originale
Peiyuan Su, Jihao Zhang, Hao Wang, Yifeng Jiang, Sharmistha Paul Dutta, Mengxu Li, Hazem Yousef, Peter Zalden, Kai Zhang, Ruixue Zhu, Xuan Liu, Yingqi Wang, Sophie E. Canton, Diana Bregenholt Jakobsen, Doriana Vinci, Wenkai Zhang, Jinggang Lan, Tsu-Chien Weng, Wenge Yang, Michael Wulff, Christopher Milne, Dmitry Khakhulin, Qingyu Kong; "Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering"; Nature Communications, Volume 17, 2026-2-9









































