Le mécanisme d'itinérance révélé par le bromoforme
Une expérience apporte la preuve de l'existence d'un mécanisme d'itinérance longtemps débattu dans les réactions photochimiques
Annonces
Le bromoforme (CHBr3), composé d'halométhane, a des effets dévastateurs sur la couche d'ozone. Dans les couches supérieures de l'atmosphère, le bromoforme réagit avec les rayons UV et libère des molécules de Brome qui détruisent les molécules d'ozone. Cependant, cette réaction a longtemps laissé les scientifiques perplexes : les molécules impliquées semblent se déplacer les unes par rapport aux autres d'une manière qui n'a pas de sens d'un point de vue énergétique. Les scientifiques de l'European XFEL ont maintenant révélé pour la première fois des preuves structurelles de ce mécanisme d'errance, l'établissant comme une caractéristique universelle des réactions photochimiques. L'étude, publiée dans Nature Communications, fournit des informations essentielles dans le domaine de la photochimie atmosphérique et sur la manière dont les composés d'halométhane tels que le bromoforme influent sur la couche d'ozone.
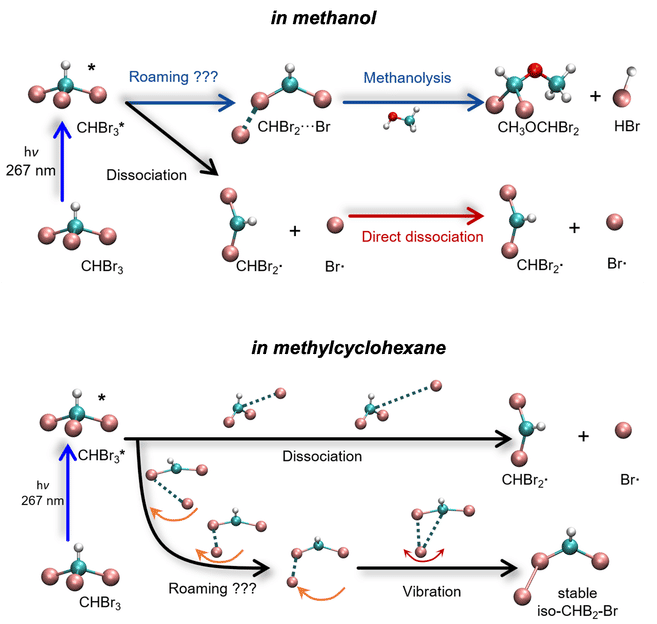
Légende : Dynamique de réaction nouvellement élucidée du bromoforme (CHBrâ'ƒ) dans les solvants méthanol (en haut) et méthylcyclohexane (en bas). Les atomes sont représentés comme suit : carbone (cyan), brome (rose), hydrogène (gris) et oxygène (rouge).
European XFEL
La couche d'ozone enveloppe la Terre à environ 15-30 km au-dessus de la surface de la planète. L'ozone absorbe les rayons ultraviolets lorsqu'ils pénètrent dans l'atmosphère, protégeant ainsi la vie sur Terre des effets des radiations nocives. Cependant, l'ozone réagit facilement avec d'autres composés présents dans la stratosphère, ce qui conduit à l'appauvrissement de la couche d'ozone et, finalement, à la création du trou d'ozone. L'un de ces composés est le bromoforme (CHBr3). Émis par les organismes marins tels que le phytoplancton et les algues, ce composé halométhane interagit avec la lumière UV lorsqu'il remonte dans les couches supérieures de l'atmosphère, en suspension dans les gouttelettes d'eau ou les aérosols. L'interaction avec la lumière UV déclenche une réaction qui aboutit à la libération de molécules de brome. Plus de 100 fois plus destructeur que d'autres gaz halogènes tels que le chlore, le brome est extrêmement réactif et détruit rapidement les molécules d'ozone. Ce sont ces types de photo-réactions qui sont à l'origine du trou d'ozone. Aujourd'hui, grâce au XFEL européen, les scientifiques ont révélé des détails structurels essentiels de ce type de réaction, améliorant ainsi notre compréhension de la chimie atmosphérique.
L'énigme des molécules itinérantes
Les détails de la réaction ultra-rapide induite par la lumière impliquant le bromoforme ont longtemps laissé les scientifiques perplexes. On sait qu'après l'interaction initiale avec la lumière UV, le bromoforme se brise en fragments, dont certains se réalignent pour former des composés chimiques stables. Cependant, curieusement, les molécules impliquées dans ces réactions ne se comportent pas comme on pourrait s'y attendre. "Des complexes intermédiaires stables sont finalement formés après la fragmentation de la bromoforme par la lumière UV", explique Qingyu Kong, scientifique au synchrotron Soleil et principal responsable de l'étude. "Toutefois, au cours des premières étapes de la réaction, ces fragments peuvent s'assembler dans des configurations structurelles qui ne semblent pas avoir de sens d'un point de vue énergétique, du moins d'un point de vue classique. Plutôt que de se séparer complètement ou de se lier d'une manière qui consomme le moins d'énergie possible, les fragments migrent lentement les uns par rapport aux autres d'une manière qui contourne les états de transition conventionnels." Pour expliquer ces observations, les scientifiques ont émis l'hypothèse de l'itinérance, qui indique que les ions semblent se déplacer plus loin pour trouver une nouvelle configuration stable. Toutefois, à ce jour, aucune preuve structurelle directe n'a été fournie pour étayer cette théorie dans le bromoforme.
Grâce au XFEL européen, une équipe de chercheurs a résolu pour la première fois ce mécanisme d'itinérance ultrarapide. Des études antérieures réalisées à l'aide de synchrotrons ont révélé les produits finaux de ces réactions, mais n'ont pas permis d'en élucider les étapes initiales. "Il était évident que la première étape cruciale de la réaction, où l'on pense que le mécanisme d'itinérance a lieu, se produit beaucoup plus rapidement que les impulsions de rayons X du synchrotron ne pouvaient le détecter", explique Dmitry Khakhulin, scientifique européen du XFEL et principal auteur de l'étude récente.
Les impulsions femtosecondes font l'affaire
Pour leur expérience, les scientifiques ont injecté des solutions de bromoforme sous forme de minces jets dans la zone d'expérience de l'instrument FXE du XFEL européen. Une impulsion laser optique femtoseconde a déclenché la réaction ; une impulsion de rayons X retardée a ensuite été utilisée pour obtenir des informations sur les différentes étapes de la réaction. Cette méthode est connue sous le nom de diffusion de rayons X en solution résolue dans le temps (femtoseconde).
Contrairement aux expériences précédentes, les impulsions de rayons X ultra-courtes générées par le XFEL européen ont permis aux scientifiques de saisir toutes les étapes structurelles de la réaction, depuis la rupture des premières liaisons et la dynamique de déplacement des fragments jusqu'à la formation de brome et de divers produits de recombinaison. Les résultats ont montré que dans les 150 femtosecondes suivant le début de la réaction, l'itinérance a eu lieu et les composés intermédiaires stables commencent à se former progressivement.
"Grâce aux impulsions de rayons X ultra-courtes générées par le XFEL européen, nous avons pu fournir pour la première fois des preuves structurelles de l'itinérance dans le bromoforme", explique M. Khakhulin.
Influence du solvant
Des études antérieures menées dans des synchrotrons ont également montré que le résultat de la réaction était influencé par le solvant. Pour leurs études à l'European XFEL, les scientifiques ont utilisé deux liquides différents comme solvants - le méthanol et le méthylcyclohexane - afin de déterminer si c'était le cas.
"Nos résultats ont montré que, bien que l'intermédiaire soit formé dans les deux liquides, ce qui se passe ensuite dépend fortement du solvant dans lequel le bromoforme est suspendu", explique M. Kong. En suspension dans le méthanol, les molécules de méthanol entraient en compétition pour se lier au composé intermédiaire, ce qui entraînait la décomposition de l'intermédiaire initial à courte durée de vie. Le méthylcyclohexane, moins réactif, a cependant permis à l'intermédiaire de se transformer en un produit stable.
"Dans l'ensemble, ces nouvelles connaissances constituent des étapes importantes vers une compréhension plus complète de la photochimie atmosphérique et offrent un nouveau cadre pour comprendre le comportement de composés tels que le bromoforme dans le contexte de l'environnement en phase gazeuse, des aérosols et des gouttelettes d'eau", conclut M. Kong.
Cette étude a été réalisée dans le cadre d'une collaboration à long terme à l'instrument FXE. Le travail a impliqué une étroite collaboration entre le XFEL européen, le synchrotron Soleil, l'université ShanghaiTech et l'ESRF.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Peiyuan Su, Jihao Zhang, Hao Wang, Yifeng Jiang, Sharmistha Paul Dutta, Mengxu Li, Hazem Yousef, Peter Zalden, Kai Zhang, Ruixue Zhu, Xuan Liu, Yingqi Wang, Sophie E. Canton, Diana Bregenholt Jakobsen, Doriana Vinci, Wenkai Zhang, Jinggang Lan, Tsu-Chien Weng, Wenge Yang, Michael Wulff, Christopher Milne, Dmitry Khakhulin, Qingyu Kong; "Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering"; Nature Communications, Volume 17, 2026-2-9














































