Le trio - nickel, palladium et platine - pour une meilleure évolution de l'hydrogène
Annonces
Selon les données du ministère de l'aménagement du territoire, des infrastructures et des transports, environ 30 000 véhicules à hydrogène seront immatriculés d'ici 2022, soit trois fois plus qu'en 2018. Cependant, le pays ne compte que 135 stations de ravitaillement en hydrogène. Afin d'améliorer l'accessibilité des véhicules à hydrogène et de faire de l'hydrogène une source d'énergie viable, il est impératif de réduire le coût de production de l'hydrogène et d'en assurer ainsi la faisabilité économique. Pour atteindre cet objectif, il est essentiel de maximiser l'efficacité de l'électrolyse et de l'évolution de l'hydrogène, le processus responsable de la production d'hydrogène à partir de l'eau.

Illustration du mécanisme du nanocatalyseur hybride à trois métaux pour l'évolution de l'hydrogène
POSTECH
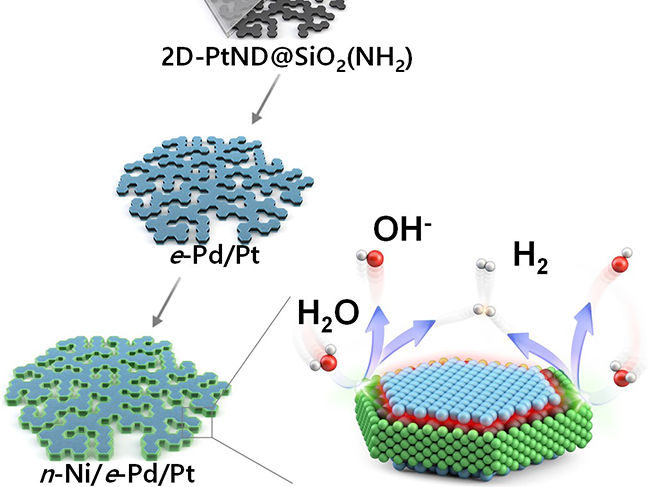
Schéma de la synthèse du catalyseur hybride à trois métaux et de l'évolution de l'hydrogène
POSTECH

Récemment, une équipe de chercheurs composée du professeur In Su Lee, du professeur de recherche Soumen Dutta et de Byeong Su Gu du département de chimie de l'université des sciences et technologies de Pohang (POSTECH) a réussi à améliorer de manière significative l'efficacité de la production d'hydrogène, une source d'énergie verte, grâce au développement d'un nanocatalyseur en platine. Ils ont accompli cette prouesse en déposant deux métaux différents de manière progressive. Les résultats de leurs recherches ont été publiés dans Angewandte Chemie, une revue réputée dans le domaine de la chimie.
Le dépôt sélectif de matériaux distincts à des endroits précis de la surface d'un catalyseur, dont la taille est de l'ordre du nanomètre, pose des problèmes considérables. Les dépôts involontaires peuvent bloquer les sites actifs du catalyseur ou interférer avec leurs fonctions respectives. Cette situation a empêché le dépôt simultané de nickel et de palladium sur un seul matériau. Le nickel est responsable de l'activation de la division de l'eau, tandis que le palladium facilite la conversion des ions hydrogène en molécules d'hydrogène.
L'équipe de recherche a mis au point un nouveau nano-réacteur pour contrôler finement l'emplacement des métaux déposés sur un nanocristal plat en 2D. En outre, ils ont conçu un processus de dépôt fin à l'échelle nanométrique, permettant de couvrir différentes facettes du nanocristal de platine 2D avec différents matériaux. Cette nouvelle approche a conduit au développement d'un matériau catalytique hybride à trois métaux "platine-nickel-palladium" obtenu par des dépôts consécutifs qui couvrent sélectivement la surface plate et le bord du nanocristal de platine 2D avec des films minces de palladium et de nickel respectivement.
Le catalyseur hybride présente des interfaces distinctes nickel/platine et palladium/platine positionnées de manière à faciliter les processus de séparation de l'eau et de génération de molécules d'hydrogène respectivement. Par conséquent, la collaboration de ces deux processus différents a considérablement renforcé l'efficacité de l'électrolyse et de l'évolution de l'hydrogène.
Les résultats de la recherche ont révélé que le nanocatalyseur hybride à trois métaux présentait une activité catalytique multipliée par 7,9 par rapport au catalyseur platine-carbone conventionnel. En outre, le nouveau catalyseur a fait preuve d'une grande stabilité, conservant son activité catalytique élevée même après un temps de réaction prolongé de 50 heures. Cela a permis de résoudre le problème des interférences fonctionnelles ou des collisions entre les hétéro-interfaces.
Le professeur In Su Lee, qui a dirigé la recherche, a exprimé son optimisme en déclarant : "Nous avons réussi à développer des hétéro-interfaces harmonieuses formées sur un matériau hybride, en surmontant les défis du processus". Il a ajouté : "J'espère que les résultats de la recherche trouveront une large application dans le développement de matériaux catalytiques optimisés pour les réactions à l'hydrogène."
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.













































