Une étape importante sur la voie de la catalyse des métaux de transition avec l'aluminium
Des chimistes réussissent à synthétiser par métathèse un sel complexe d'aluminium cationique de faible valence
Les chimistes Philipp Dabringhaus, Julie Willrett et le professeur Ingo Krossing de l'Institut de chimie inorganique et analytique de l'Université de Fribourg ont réussi à synthétiser le complexe d'aluminium cationique de faible valeur [Al(AlCp*)3]+ par une réaction de métathèse. L'équipe présente ses travaux de recherche dans la revue Nature Chemistry.
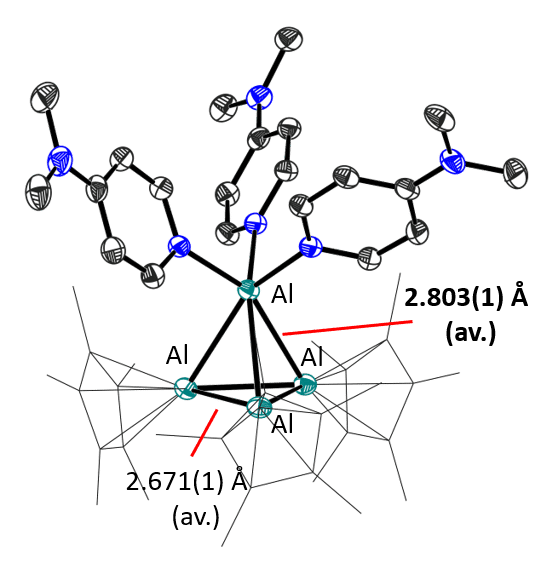
L'ajout de ligands, comme la diméthylaminopyridine dans ce cas, brise la structure dimérique du cation et l'atome d'aluminium solitaire montre son fort caractère accepteur.
Image: provided by the research group
"En chimie, les composés cationiques d'aluminium de faible valence sont très recherchés en raison de leur réactivité ambiphile potentielle de type métal de transition. Cependant, de nombreuses tentatives antérieures de synthèse de composés cationiques d'aluminium de faible valence par des méthodes oxydatives ou réductrices ont été largement infructueuses", explique Krossing. Jusqu'à présent, dit-il, il n'y a eu qu'un seul exemple de composé cationique d'aluminium de faible valence, mais il ne peut être préparé par synthèse rationnelle. "Nous montrons maintenant qu'il existe un accès étonnamment facile aux complexes d'aluminium de faible valence grâce à la métathèse", déclare Krossing. Dans la métathèse, les structures partielles sont simplement échangées entre les partenaires de la réaction.
L'aluminium, une alternative moins chère pour la catalyse
Les chimistes de Fribourg ont préparé le sel [Al(AlCp*)3]+[Al(OC{CF3)3}4]- à partir du tétramère de Schnöckel (AlCp*)4, dans lequel l'aluminium est déjà présent au degré d'oxydation +1. Le (AlCp*)4 a réagi avec Li[Al{OC(CF3)3}4] et le mélange réactionnel est immédiatement passé du jaune au rouge. Lorsque le mélange réactionnel a été cristallisé, les scientifiques ont obtenu le sel [Al(AlCp*)3]+[Al(OC{CF3)3}4] sous forme de cristaux violet foncé. "Les études de cristallographie aux rayons X, de spectrométrie UV et de calcul indiquent la présence de la structure dimérique à la fois à l'état solide et en solution à haute concentration et à basse température, mais à faible concentration et à température ambiante, le monomère se forme. Cela indique clairement une réactivité ambiphile du cation", a déclaré M. Dabringhaus.
"Par conséquent, ce sel peut potentiellement être utilisé comme élément de base pour un sel [:Al(L)3]+ qui, en raison de sa nature cationique, pourrait être capable d'effectuer des additions oxydatives et des éliminations réductrices réversibles de petites molécules", explique Krossing. "Cela nous rapproche un peu plus de notre objectif à long terme, qui est de réaliser la catalyse - actuellement effectuée avec des métaux de transition coûteux et rares - avec de l'aluminium. L'aluminium est le deuxième élément le plus abondant de la croûte terrestre et il en est capable en principe, comme le montrent nos travaux. Mais malheureusement, il faudra probablement attendre encore au moins 20 ans avant que nos recherches dans ce domaine ne soient appliquées."
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.