Un nouveau concept pour des batteries à faible coût
La nouvelle technologie constitue déjà la base d'une nouvelle entreprise dérivée.
Alors que le monde se dote d'installations éoliennes et solaires de plus en plus importantes, le besoin de systèmes de secours économiques et à grande échelle pour fournir de l'énergie lorsque le soleil est couché et que l'air est calme se fait rapidement sentir. Les batteries lithium-ion actuelles sont encore trop chères pour la plupart de ces applications, et d'autres options telles que l'hydroélectricité par pompage nécessitent une topographie spécifique qui n'est pas toujours disponible.

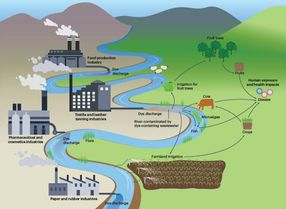
Les trois principaux constituants de la batterie sont : à gauche, l'aluminium ; au centre, le soufre ; et à droite, les cristaux de sel gemme. Tous ces matériaux sont disponibles sur place et abondent sur Terre, sans nécessiter de chaîne d'approvisionnement mondiale.
Rebecca Miller
Des chercheurs du MIT et d'ailleurs ont mis au point un nouveau type de batterie, entièrement fabriquée à partir de matériaux abondants et peu coûteux, qui pourrait contribuer à combler cette lacune.
La nouvelle architecture de la batterie, qui utilise l'aluminium et le soufre comme deux matériaux d'électrode, avec un électrolyte de sel fondu entre les deux, est décrite dans la revue Nature, dans un article du professeur Donald Sadoway du MIT, ainsi que de 15 autres personnes du MIT et de Chine, du Canada, du Kentucky et du Tennessee.
"Je voulais inventer quelque chose qui soit meilleur, bien meilleur, que les batteries lithium-ion pour le stockage stationnaire à petite échelle et, à terme, pour l'automobile", explique M. Sadoway, professeur émérite de chimie des matériaux John F. Elliott.
En plus d'être coûteuses, les batteries au lithium-ion contiennent un électrolyte inflammable, ce qui ne les rend pas idéales pour le transport. M. Sadoway a donc commencé à étudier le tableau périodique, à la recherche de métaux bon marché, abondants sur Terre, qui pourraient remplacer le lithium. Selon lui, le métal dominant sur le plan commercial, le fer, ne possède pas les propriétés électrochimiques nécessaires à une batterie efficace. Mais le deuxième métal le plus abondant sur le marché - et en fait le métal le plus abondant sur Terre - est l'aluminium. "Alors, j'ai dit, eh bien, faisons en sorte que ce soit un complément. Ce sera de l'aluminium", dit-il.
Il a ensuite fallu décider avec quoi associer l'aluminium à l'autre électrode, et quel type d'électrolyte mettre entre les deux pour transporter les ions pendant la charge et la décharge. Le soufre étant le moins cher de tous les non-métaux, il est devenu le matériau de la deuxième électrode. Quant à l'électrolyte, "nous n'allions pas utiliser les liquides organiques volatils et inflammables" qui ont parfois provoqué des incendies dangereux dans les voitures et d'autres applications des batteries lithium-ion, explique M. Sadoway. Ils ont essayé certains polymères, mais ont fini par se tourner vers une variété de sels fondus qui ont des points de fusion relativement bas - proches du point d'ébullition de l'eau, par opposition à près de 1 000 degrés Fahrenheit pour de nombreux sels. "Dès que l'on descend à une température proche de celle du corps, il devient pratique" de fabriquer des batteries qui ne nécessitent pas d'isolation spéciale ni de mesures anticorrosion, explique-t-il.
Les trois ingrédients qu'ils ont trouvés sont bon marché et facilement disponibles : l'aluminium, qui n'est pas différent du papier d'aluminium que l'on trouve au supermarché, le soufre, qui est souvent un déchet de processus tels que le raffinage du pétrole, et des sels largement disponibles. "Les ingrédients sont bon marché et le produit est sûr : il ne peut pas brûler", explique M. Sadoway.
Au cours de leurs expériences, les membres de l'équipe ont montré que les cellules de la batterie pouvaient supporter des centaines de cycles à des taux de charge exceptionnellement élevés, avec un coût prévu par cellule d'environ un sixième de celui des cellules lithium-ion comparables. Ils ont montré que le taux de charge dépendait fortement de la température de travail, 110 degrés Celsius (230 degrés Fahrenheit) présentant des taux 25 fois plus rapides que 25 C (77 F).
Étonnamment, le sel fondu que l'équipe a choisi comme électrolyte simplement en raison de son faible point de fusion s'est avéré avoir un avantage fortuit. L'un des principaux problèmes de fiabilité des batteries est la formation de dendrites, c'est-à-dire d'étroites pointes de métal qui s'accumulent sur une électrode et finissent par se développer pour entrer en contact avec l'autre électrode, ce qui provoque un court-circuit et nuit à l'efficacité. Mais il se trouve que ce sel particulier est très efficace pour prévenir ce dysfonctionnement.
Le sel de chloro-aluminate qu'ils ont choisi "met essentiellement fin à ces dendrites fugitives, tout en permettant une charge très rapide", explique M. Sadoway. "Nous avons fait des expériences à des taux de charge très élevés, en chargeant en moins d'une minute, et nous n'avons jamais perdu de cellules à cause du court-circuitage des dendrites."
"C'est drôle", ajoute-t-il, car tout l'objectif était de trouver un sel ayant le point de fusion le plus bas, mais les chloro-aluminates caténés qu'ils ont fini par obtenir se sont révélés résistants au problème de court-circuit. "Si nous avions commencé par essayer d'empêcher le court-circuitage dendritique, je ne suis pas sûr que j'aurais su comment poursuivre dans cette voie", dit M. Sadoway. "Je suppose que c'était une sérendipité pour nous".
Qui plus est, la batterie ne nécessite aucune source de chaleur externe pour maintenir sa température de fonctionnement. La chaleur est naturellement produite par voie électrochimique lors de la charge et de la décharge de la batterie. "Lorsque vous chargez, vous générez de la chaleur, ce qui empêche le sel de geler. Puis, lorsque vous déchargez, vous générez également de la chaleur", explique M. Sadoway. Dans une installation typique utilisée pour le nivellement de la charge d'une centrale solaire, par exemple, "vous stockez l'électricité lorsque le soleil brille, puis vous la prélevez à la tombée de la nuit, et vous faites cela tous les jours. Et cette alternance charge-ralenti-décharge-ralenti est suffisante pour générer suffisamment de chaleur pour maintenir la chose à température."
Selon lui, cette nouvelle formulation de batterie serait idéale pour des installations de la taille nécessaire à l'alimentation d'une seule maison ou d'une petite ou moyenne entreprise, produisant une capacité de stockage de l'ordre de quelques dizaines de kilowattheures.
Pour des installations plus importantes, jusqu'à l'échelle d'un service public de dizaines ou de centaines de mégawatts-heure, d'autres technologies pourraient être plus efficaces, notamment les batteries à métal liquide que M. Sadoway et ses étudiants ont développées il y a plusieurs années et qui ont servi de base à une entreprise dérivée appelée Ambri, qui espère livrer ses premiers produits au cours de l'année prochaine. Pour cette invention, M. Sadoway a récemment reçu le prix de l'inventeur européen de cette année.
Selon M. Sadoway, la plus petite échelle des batteries aluminium-soufre les rendrait également pratiques pour des utilisations telles que les stations de recharge de véhicules électriques. Il fait remarquer que lorsque les véhicules électriques seront suffisamment répandus sur les routes pour que plusieurs voitures veuillent se recharger en même temps, comme c'est le cas aujourd'hui avec les pompes à essence, "si vous essayez de le faire avec des batteries et que vous voulez une charge rapide, les ampérages sont tellement élevés que nous n'avons pas cette quantité d'ampérage dans la ligne qui alimente l'installation". Le fait de disposer d'un système de batteries tel que celui-ci pour stocker l'énergie et la restituer rapidement en cas de besoin pourrait donc éliminer la nécessité d'installer de nouvelles lignes électriques coûteuses pour desservir ces chargeurs.
La nouvelle technologie est déjà à la base d'une nouvelle entreprise dérivée appelée Avanti, qui a obtenu une licence pour les brevets du système, cofondée par Sadoway et Luis Ortiz '96 ScD '00, qui était également cofondateur d'Ambri. "Le premier objectif de l'entreprise est de démontrer que le système fonctionne à grande échelle", explique M. Sadoway, puis de le soumettre à une série de tests de résistance, notamment à des centaines de cycles de charge.
Une batterie à base de soufre risquerait-elle de produire les mauvaises odeurs associées à certaines formes de soufre ? Aucune chance, selon M. Sadoway. "L'odeur d'œuf pourri se trouve dans le gaz, le sulfure d'hydrogène. C'est du soufre élémentaire, et il va être enfermé dans les cellules." Si vous essayez d'ouvrir une pile au lithium-ion dans votre cuisine, dit-il (et n'essayez pas de le faire chez vous !), "l'humidité de l'air réagirait et vous commenceriez à produire toutes sortes de gaz nocifs". Ces questions sont légitimes, mais la batterie est scellée, ce n'est pas un récipient ouvert. Je ne m'inquiéterais donc pas à ce sujet".
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Autres actualités du département science
Actualités les plus lues
Plus actualités de nos autres portails
Il se trame quelque chose dans l'industrie chimique…
Voilà à quoi ressemble le véritable esprit pionnier : De nombreuses start-ups innovantes apportent des idées fraîches, de la passion et un esprit d'entreprise pour changer positivement le monde de demain. Plongez dans l'univers de ces jeunes entreprises et profitez de la possibilité d'entrer en contact avec leurs fondateurs.