Libertar o poder do ouro: um avanço na química verde
Os investigadores descobriram uma poderosa sinergia entre o ouro, o manganésio e o cobre que poderá transformar a forma como produzimos produtos químicos valiosos
Anúncios
O acetaldeído é um intermediário químico fundamental, tradicionalmente produzido através do processo de oxidação Wacker baseado no etileno, que é dispendioso e prejudicial para o ambiente. A oxidação selectiva do bioetanol em acetaldeído constitui uma alternativa mais ecológica e sustentável, mas a maior parte dos catalisadores existentes depara-se com o habitual compromisso entre atividade e seletividade, produzindo normalmente menos de 90% de acetaldeído.
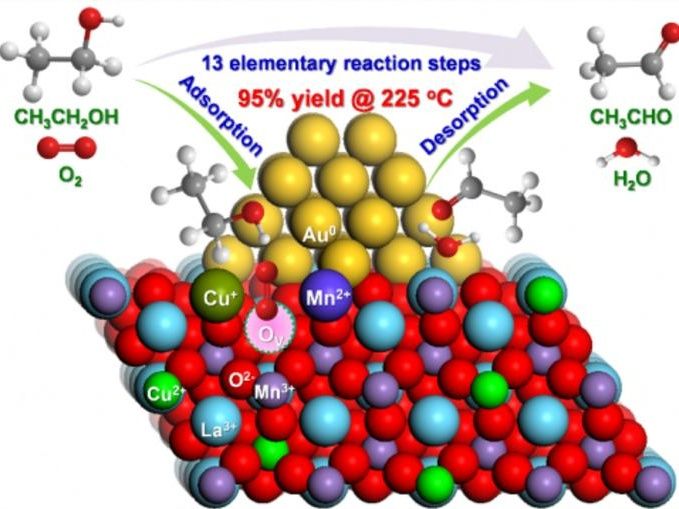
Os investigadores descobriram uma poderosa sinergia entre o ouro, o manganês e o cobre que poderá transformar a forma como produzimos produtos químicos valiosos. Apoiando minúsculas nanopartículas de ouro num material de perovskite especialmente concebido (LaMn0,75Cu0,25O3), a equipa conseguiu um rendimento impressionante de 95% de acetaldeído a partir do etanol a apenas 225 °C, um passo importante para processos químicos mais limpos e mais eficientes. O segredo está na utilização inteligente do cobre. Uma pequena quantidade de Cu melhora drasticamente o catalisador ao criar sítios activos que aceleram a etapa mais difícil da reação. Mas há um senão: demasiado cobre desestabiliza o sistema, reduzindo a eficiência. Este delicado equilíbrio realça a importância da conceção a nível atómico dos catalisadores da próxima geração para o fabrico sustentável de produtos químicos.
Chinese Journal of Catalysis
Nomeadamente, Liu e Hensen demonstraram uma sinergia específica Au0-Cu+ no catalisador Au/MgCuCr2O4 de última geração, obtendo um rendimento superior a 95% de AC a 250oCcom um desempenho estável durante mais de 500 horas (J. Am. Chem. Soc. 2013, 135, 14032; J. Catal. 2015, 331, 138; J. Catal. 2017, 347, 45). Apesar deste passo significativo dado há mais de uma década, a procura de catalisadores mais eficientes, não tóxicos e capazes de promover a oxidação selectiva do etanol a temperaturas mais baixas continua a ser um grande desafio.
Recentemente, a equipa de investigação liderada pelo Prof. Peng Liu (Universidade de Ciência e Tecnologia de Huazhong) e pelo Prof. Emiel J.M. Hensen (Universidade de Tecnologia de Eindhoven) comunicou progressos significativos na oxidação selectiva do etanol. Desenvolveram uma série de catalisadores Au/LaMnCuO3 com diferentes rácios Mn/Cu, entre os quais a composição Au/LaMn0,75Cu0,25O3 exibiu um efeito sinérgico pronunciado entre as nanopartículas de ouro e a perovskite LaMnO3 moderadamente dopada com Cu. Esta sinergia permitiu uma oxidação eficiente do etanol a menos de 250oC, superando o desempenho do catalisador Au/MgCuCr2O4 anteriormente avaliado. Os resultados foram publicados no Chinese Journal of Catalysis.
Para melhorar a eficiência da conversão de bioetanol em acetaldeído - um químico valioso utilizado em plásticos e produtos farmacêuticos, os investigadores desenvolveram uma nova classe de catalisadores baseados em materiais de perovskite. Estes suportes foram sintetizados através de um método de combustão sol-gel e depois revestidos com nanopartículas de ouro. Ajustando a relação entre o manganês e o cobre na estrutura da perovskite, a equipa identificou uma composição óptima (Au/LaMn0,75Cu0,25O3) que atingiu um rendimento elevado de acetaldeído de 95% a 225°C e manteve um desempenho estável durante 80 horas. Os catalisadores com maior teor de cobre foram menos eficazes, em grande parte porque o cobre tende a perder a sua forma ativa durante a reação. O melhor desempenho do catalisador optimizado está ligado a uma interação cooperativa entre os iões de ouro, manganês e cobre.
Para compreender melhor o modo como estes elementos funcionam em conjunto, os investigadores utilizaram técnicas computacionais avançadas, incluindo a teoria funcional da densidade e simulações microcinéticas. Estes estudos revelaram que a dopagem do cobre na perovskite cria sítios activos perto das partículas de ouro que ajudam a ativar as moléculas de oxigénio e etanol de forma mais eficiente. O catalisador optimizado também apresentou uma barreira de energia mais baixa para as principais etapas da reação, tornando o processo mais eficiente. Tanto os resultados experimentais como os teóricos realçam a importância de afinar a composição do catalisador para obter um melhor desempenho.
Observação: Este artigo foi traduzido usando um sistema de computador sem intervenção humana. A LUMITOS oferece essas traduções automáticas para apresentar uma gama mais ampla de notícias atuais. Como este artigo foi traduzido com tradução automática, é possível que contenha erros de vocabulário, sintaxe ou gramática. O artigo original em Inglês pode ser encontrado aqui.