Une nouvelle réaction ammoniacale pourrait permettre de disposer d'une source d'azote durable
Nouveau système d'activation et de transfert catalytique de l'ammoniac - La catalyse est basée sur les éléments des groupes principaux
Annonces
L'un des grands objectifs de la chimie est de produire facilement des amines à partir d'Ammoniac et d'hydrocarbures insaturés. L'addition catalytique, au cours de laquelle l'ammoniac est activé puis transféré, ne produit en outre aucun déchet, ce qui la rend particulièrement durable. Des chercheurs de l'Institut de technologie de Karlsruhe (KIT) se sont désormais rapprochés de l'objectif. Ils ont développé un système d'activation et de transfert catalytique de l'ammoniac qui n'est pas basé sur des métaux de transition, mais sur un composé d'éléments du groupe principal.
La molécule d'ammoniac (NH3), un composé d'azote et d'hydrogène, est l'une des substances chimiques les plus produites au monde et constitue la matière première pour la fabrication de nombreux autres composés azotés. Si l'on parvenait à produire facilement des amines en ajoutant de l'ammoniac à des hydrocarbures insaturés, la chimie ferait une percée décisive. En effet, les amines, des dérivés organiques de l'ammoniac, sont demandées dans de nombreux domaines différents : elles servent par exemple de composants pour les produits agrochimiques et pharmaceutiques ainsi que pour les substances actives de lavage, les colorants, les lubrifiants et les revêtements. Les amines sont également utilisées comme catalyseurs dans la production de polyuréthanes. Une autre application importante est le lavage des gaz dans les raffineries et les centrales électriques.
En brisant la forte liaison entre l'azote et l'hydrogène, ce que l'on appelle l'activation, la molécule d'ammoniac peut, du moins en théorie, être transférée à d'autres molécules comme les hydrocarbures insaturés. Par exemple, le transfert d'ammoniac sur l'alcène éthylène, une substance importante dans l'industrie chimique, produirait de l'éthylamine. Les chimistes désignent cette addition par le terme d'hydroamination. Cependant, l'ammoniac et l'éthylène ne réagissent pas simplement l'un avec l'autre - un catalyseur doit servir d'intermédiaire à la réaction. Or, les catalyseurs habituels et ceux à base de métaux de transition ont l'inconvénient de réagir eux-mêmes avec l'ammoniac et de devenir ainsi inactifs. "L'hydroamination d'alcènes non activés par l'ammoniac est donc considérée comme un grand défi, pour ainsi dire comme le Saint Graal de la catalyse", explique le professeur Frank Breher, chef de groupe de recherche du département de chimie moléculaire à l'Institut de chimie inorganique (AOC) du KIT.
Activation et transfert catalytique de l'ammoniac
Le professeur Frank Breher et le Dr Felix Krämer de l'AOC du KIT, soutenus par des chercheurs de l'université de Paderborn et de l'université Complutense de Madrid, se sont désormais rapprochés de cet objectif ambitieux. "Nous avons développé un système d'activation de l'ammoniac qui n'est pas basé sur les métaux de transition, mais sur les éléments des groupes principaux. Aucun déchet n'est produit lors du processus d'activation et de transfert ultérieur de l'ammoniac, ce qui est bien sûr particulièrement intéressant du point de vue de la durabilité", explique Breher. Les chercheurs ont publié un rapport sur leurs travaux dans la revue Nature Chemistry.
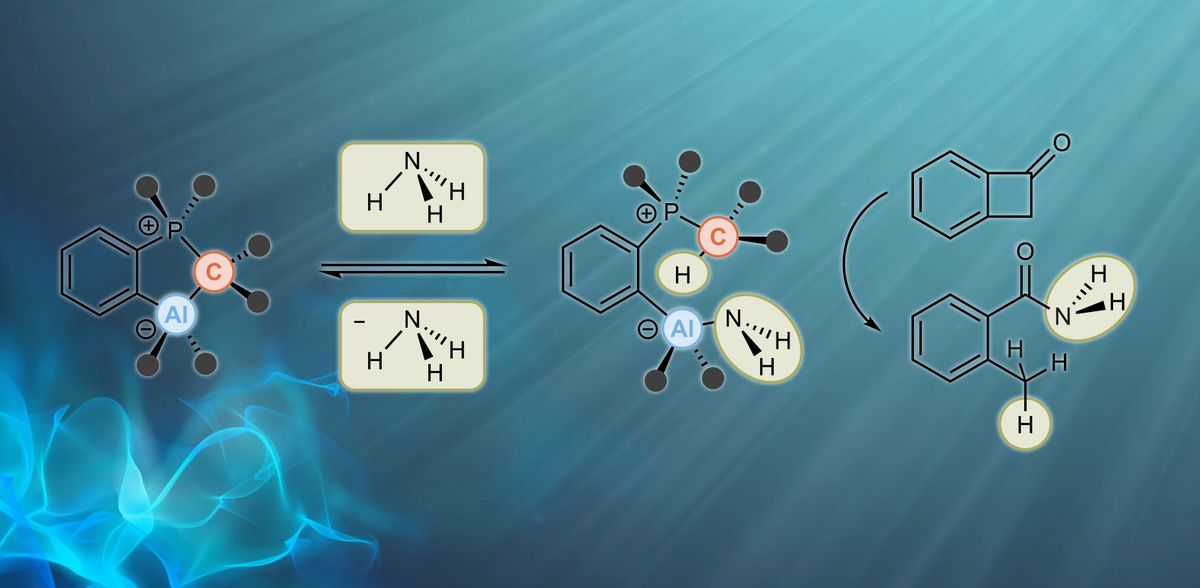
L'équipe a créé ce que l'on appelle une paire de Lewis frustrée (FLP), composée d'un acide comme accepteur de paires d'électrons et d'une base comme donneur de paires d'électrons. Les deux réagissent généralement l'un avec l'autre et produisent un adduit. Si la formation d'adduits est empêchée ou du moins limitée, il en résulte pour ainsi dire une situation de frustration et la molécule réagit volontiers avec de petites molécules comme l'ammoniac. "Il est toutefois décisif d'atténuer la réactivité de manière à ce que la réaction avec les petites molécules soit la plus réversible possible, car ce n'est qu'à cette condition qu'il est possible d'utiliser un tel FLP dans la catalyse. Nous y sommes parvenus pour la première fois avec de l'ammoniac comme substrat", rapporte Breher. Les chercheurs ont montré que le composé titre réagit facilement avec l'ammoniac non aqueux de manière thermoneutre et qu'il clive de manière réversible la liaison azote-hydrogène de l'ammoniac à température ambiante. En outre, dans leur publication, ils présentent pour la première fois des réactions de transfert de NH3 médiées par un catalyseur à base d'éléments du groupe principal. "Certes, nous n'avons jusqu'à présent converti que des substrats activés et pas encore d'hydrocarbures insaturés, mais nous nous sommes nettement rapprochés de la 'réaction de rêve'", déclare Breher. "Nous nous attendons à ce que notre première preuve de principe déclenche d'autres travaux sur l'utilisation de l'ammoniac activé par N-H comme source d'azote facilement disponible et durable".
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Allemand peut être trouvé ici.



![Catalyse de la [Fe]-hydrogénase visualisée à l'aide de la spectroscopie de résonance magnétique nucléaire rehaussée de para-hydrogène](https://img.chemie.de/Portal/News/675fd46b9b54f_sBuG8s4sS.png?tr=w-712,h-534,cm-extract,x-0,y-16:n-zoom)








































