Capturer le CO2 avec de l'électricité : une enzyme microbienne inspire l'électrochimie
Vers une nouvelle solution pour l'utilisation du CO2 atmosphérique
Annonces
L'homme émet continuellement des gaz à effet de serre, ce qui aggrave le réchauffement de la planète. Par exemple, le dioxyde de carbone (CO2) s'accumule considérablement au fil des ans et est chimiquement très stable. Pourtant, certains microbes capturent le CO2 à l'aide d'enzymes très efficaces. Des scientifiques de l'Institut Max Planck de microbiologie marine de Brême et des universités de Genève et de Radboud ont isolé l'une de ces enzymes. Lorsque l'enzyme est branchée électroniquement sur une électrode, ils observent la conversion du CO2 en formiate avec une efficacité parfaite. Ce phénomène inspirera de nouveaux systèmes de fixation du CO2 en raison de sa directionnalité et de ses taux remarquables. Les résultats sont maintenant publiés dans "Angewandte Chemie".
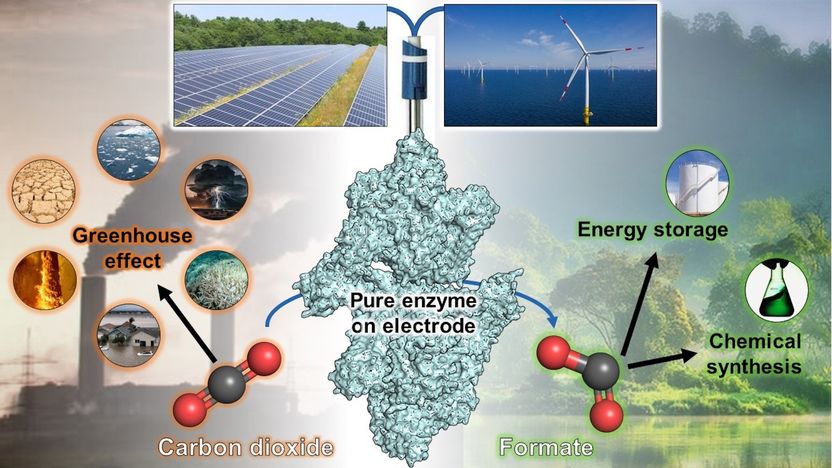
Le processus de conversion des gaz par une réaction enzymatique à base d'électrodes
Computer-generated image
À la recherche de micro-organismes capables de capturer efficacement le CO2, un gaz à effet de serre
"Les enzymes utilisées par les micro-organismes représentent un fantastique terrain de jeu pour les scientifiques, car elles permettent des réactions hautement spécifiques à des vitesses rapides", explique Tristan Wagner, directeur du groupe de recherche Max Planck sur le métabolisme microbien à l'Institut Max Planck de microbiologie marine (MPIMM). Certaines de ces enzymes ont une façon intéressante de capturer le CO2 : Elles le transforment en formiate, un composé stable et sûr qui peut être utilisé pour stocker de l'énergie ou pour synthétiser diverses molécules à des fins industrielles ou pharmaceutiques. Un exemple est Methermicoccus shengliensis, un méthanogène (microbe produisant du méthane) isolé d'un gisement de pétrole et se développant à 50 °C. Il a été cultivé et étudié pendant plus de dix ans. Il a été cultivé et étudié ces dernières années par Julia Kurth et Cornelia Welte à l'université Radboud aux Pays-Bas. À l'Institut Max Planck de microbiologie marine, Olivier Lemaire, Mélissa Belhamri et Tristan Wagner ont disséqué le microbe pour trouver son enzyme de capture du CO2 et mesurer la rapidité et l'efficacité avec lesquelles il peut transformer le CO2.
Une enzyme de conversion du CO2 à fort potentiel
Les scientifiques de Max Planck ont entrepris la tâche difficile d'isoler l'enzyme microbienne. "Comme nous savions que ces enzymes sont sensibles à l'oxygène, nous avons dû travailler à l'intérieur d'une tente anaérobie dépourvue d'air ambiant pour la séparer des autres protéines - c'était assez compliqué, mais nous avons réussi", explique Olivier Lemaire. Une fois isolée, les scientifiques ont caractérisé les propriétés de l'enzyme. Ils ont montré qu'elle génère efficacement du formiate à partir du CO2, mais qu'elle effectue la réaction inverse à une vitesse très lente et avec un faible rendement. "Les enzymes similaires appartenant à la famille des formiate déshydrogénases sont bien connues pour fonctionner dans les deux sens, mais nous avons montré que l'enzyme de Methermicoccus shengliensis est presque unidirectionnelle et ne pouvait pas convertir efficacement le formiate en CO2", rapporte Mélissa Belhamri. "Ce phénomène, qui ne se produit qu'en l'absence d'oxygène, nous a enthousiasmés", ajoute-t-elle. "Comme le formiate généré par la fixation du CO2 ne peut pas être retransformé et s'accumule donc, un tel système serait un candidat très intéressant pour la capture du CO2, surtout si nous pouvions le brancher sur une électrode", souligne Tristan Wagner. L'avantage : L'enzyme étant naturellement ou chimiquement attachée à une électrode, l'"énergie" nécessaire à la capture du CO2 sera directement fournie par l'électrode, sans perte de courant électrique ni nécessité de recourir à des composés chimiques coûteux ou toxiques en guise de relais. Par conséquent, les électrodes liées à l'enzyme sont des systèmes efficaces et attrayants pour les procédures de conversion de gaz. L'enzyme purifiée a donc été envoyée à l'Université de Genève pour mettre en place un système de capture du CO2 basé sur des électrodes.
Conversion des gaz à l'électricité
Selmihan Sahin et Ross Milton de l'Université de Genève sont des spécialistes de l'électrochimie. Ils utilisent des électrodes reliées à un courant électrique pour effectuer des réactions chimiques. La production de formiate à partir de CO2 par électrodes nécessite souvent des métaux polluants et rares. C'est pourquoi ils ont essayé de remplacer ces métaux par l'enzyme extraite dans le groupe de Tristan Wagner au MPIMM. La procédure de fixation de l'enzyme sur une électrode n'est pas toujours aussi efficace que prévu, mais l'enzyme du groupe de recherche de Wagner possède des caractéristiques spécifiques qui pourraient faciliter le processus. Les scientifiques suisses ont réussi à fixer l'enzyme sur une électrode de graphite, où elle a effectué la conversion du gaz. Les taux mesurés étaient comparables à ceux obtenus avec des formiate déshydrogénases classiques. "La force de ce système biologique couplé à l'électrode réside dans son efficacité à transférer les électrons de l'électricité vers la transformation du CO2", souligne Lemaire. Sahin et Milton ont également confirmé que le système effectue mal la réaction inverse, comme cela avait été observé précédemment dans le tube de réaction. Par conséquent, l'électrode modifiée a converti en continu le gaz à effet de serre en formiate sans qu'aucun produit secondaire détectable ne soit généré ou que le courant électrique ne soit perdu.
Vers une nouvelle solution pour l'utilisation du CO2 atmosphérique
Ce travail de collaboration offre un nouvel outil moléculaire à la communauté scientifique : Une enzyme qui convertit le CO2 en transférant de l'électricité avec une grande efficacité. L'énergie verte renouvelable (éolienne ou solaire, par exemple) pourrait fournir de l'électricité au système à base d'électrodes qui transformerait le CO2 en formiate, une molécule directement utilisable pour des applications ou pour stocker de l'énergie. "Avant nous, personne n'avait essayé d'étudier une enzyme provenant d'un tel méthanogène pour une conversion de gaz basée sur une électrode", explique Tristan Wagner. "Pourtant, les méthanogènes sont des convertisseurs de gaz naturels exceptionnels". Aussi puissantes qu'elles puissent être, l'utilisation d'enzymes pour des processus à grande échelle nécessiterait également des systèmes de production d'enzymes à échelle similaire, ce qui représente un investissement considérable. Par conséquent, bien que la stratégie découverte puisse, en théorie, améliorer considérablement la transformation du CO2, une connaissance approfondie du mécanisme enzymatique est nécessaire avant son application, et l'équipe de chercheurs va maintenant devoir disséquer en profondeur les secrets moléculaires de la réaction.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.











































