Platine liquide à température ambiante
Le catalyseur "cool" d'une révolution durable dans la chimie industrielle
Des chercheurs australiens ont réussi à utiliser des traces de platine liquide pour créer des réactions chimiques bon marché et très efficaces à basse température, ouvrant ainsi la voie à une réduction spectaculaire des émissions dans des secteurs cruciaux.

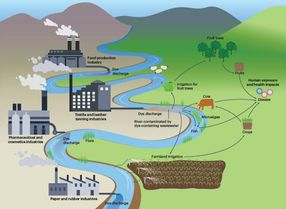
Gallium liquide et trois billes solides de platine, démontrant le processus de dissolution du platine dans le gallium décrit dans l'article de recherche.
Dr Md. Arifur Rahim, UNSW Sydney

Une vue atomique du système catalytique dans lequel les sphères argentées représentent les atomes de gallium et les sphères rouges les atomes de platine. Les petites sphères vertes sont les réactifs et les sphères bleues sont les produits - mettant en évidence les réactions catalytiques.
Dr Md. Arifur Rahim, UNSW Sydney

Perles de gallium et de platine liquides en gros plan.
Dr Md. Arifur Rahim, UNSW Sydney



Combinées au gallium liquide, les quantités de platine requises sont suffisamment faibles pour accroître de manière significative les réserves terrestres de ce métal précieux, tout en offrant potentiellement des solutions plus durables pour la réduction du CO2, la synthèse de l'ammoniac dans la production d'engrais et la création de piles à combustible vertes, ainsi que de nombreuses autres applications possibles dans les industries chimiques.
Ces résultats, qui portent sur le platine, ne sont qu'une goutte d'eau dans l'océan des métaux liquides en ce qui concerne le potentiel de ces systèmes de catalyse. En développant cette méthode, il pourrait y avoir plus de 1 000 combinaisons d'éléments possibles pour plus de 1 000 réactions différentes.
Le platine est très efficace en tant que catalyseur (le déclencheur de réactions chimiques), mais il n'est pas très utilisé à l'échelle industrielle en raison de son coût. La plupart des systèmes de catalyse faisant appel au platine ont également des coûts énergétiques permanents élevés pour fonctionner.
Normalement, le point de fusion du platine est de 1700°C. Et lorsqu'il est utilisé à l'état solide à des fins industrielles, un système catalytique à base de carbone doit contenir environ 10 % de platine.
Ce ratio n'est pas abordable lorsqu'il s'agit de fabriquer des composants et des produits destinés à la vente commerciale.
Cela pourrait toutefois changer à l'avenir, après que des scientifiques de l'UNSW Sydney et de l'université RMIT ont trouvé un moyen d'utiliser de minuscules quantités de platine pour créer des réactions puissantes, et ce sans coûts énergétiques élevés.
L'équipe, qui comprend des membres du Centre d'excellence de l'ARC pour la science des excitons et du Centre d'excellence de l'ARC pour les futures technologies à faible énergie, a combiné le platine avec du gallium liquide, dont le point de fusion n'est que de 29,8 °C, soit la température ambiante d'une journée chaude. Lorsqu'il est combiné au gallium, le platine devient soluble. En d'autres termes, il fond, sans qu'il soit nécessaire d'allumer un four industriel extrêmement puissant.
Pour ce mécanisme, le traitement à une température élevée n'est nécessaire qu'au stade initial, lorsque le platine est dissous dans le gallium pour créer le système de catalyse. Et même dans ce cas, la température n'est que d'environ 300°C pendant une heure ou deux, ce qui est loin des hautes températures continues souvent requises dans le génie chimique à l'échelle industrielle.
L'auteur collaborateur, le Dr Jianbo Tang de l'UNSW, compare cette méthode à celle d'un forgeron utilisant une forge chaude pour fabriquer des équipements qui dureront des années.
"Si vous travaillez avec du fer et de l'acier, vous devez le chauffer pour fabriquer un outil, mais vous avez l'outil et vous ne devez plus jamais le chauffer à nouveau", a-t-il déclaré.
"D'autres personnes ont essayé cette approche, mais elles doivent faire fonctionner leurs systèmes de catalyse à des températures très élevées en permanence."
Pour créer un catalyseur efficace, les chercheurs ont dû utiliser un rapport de moins de 0,0001 entre le platine et le gallium. Et le plus remarquable, c'est que le système résultant s'est avéré plus de 1 000 fois plus efficace que son rival à l'état solide (celui qui avait besoin d'environ 10 % de platine cher pour fonctionner).
Les avantages ne s'arrêtent pas là : comme il s'agit d'un système liquide, il est également plus fiable. Les systèmes catalytiques à l'état solide finissent par s'encrasser et cesser de fonctionner. Ce n'est pas un problème ici. Comme un jeu d'eau avec une fontaine intégrée, le mécanisme liquide se rafraîchit constamment, autorégulant son efficacité sur une longue période et évitant l'équivalent catalytique de l'écume de l'étang qui se forme à la surface.
Le Dr Md. Arifur Rahim, l'auteur principal de l'UNSW Sydney, a déclaré : "Depuis 2011, les scientifiques ont pu miniaturiser les systèmes catalytiques jusqu'au niveau atomique des métaux actifs. Pour maintenir les atomes uniques séparés les uns des autres, les systèmes conventionnels nécessitent des matrices solides (comme le graphène ou l'oxyde métallique) pour les stabiliser. J'ai pensé, pourquoi ne pas utiliser plutôt une matrice liquide et voir ce qui se passe.
"Les atomes catalytiques ancrés sur une matrice solide sont immobiles. Nous avons ajouté de la mobilité aux atomes catalytiques à basse température en utilisant une matrice liquide de gallium".
Le mécanisme est également suffisamment polyvalent pour effectuer des réactions d'oxydation et de réduction, dans lesquelles l'oxygène est respectivement fourni ou retiré d'une substance.
Les expérimentateurs de l'UNSW ont dû résoudre certains mystères pour comprendre ces résultats impressionnants. Grâce à une chimie computationnelle et une modélisation avancées, leurs collègues du RMIT, dirigés par le professeur Salvy Russo, ont pu identifier que le platine ne devient jamais solide, jusqu'au niveau des atomes individuels.
Le Dr Nastaran Meftahi, chercheur en science des excitons, a révélé l'importance du travail de modélisation de son équipe du RMIT.
"Ce que nous avons découvert, c'est que les deux atomes de platine ne sont jamais entrés en contact l'un avec l'autre", a-t-elle déclaré.
"Ils étaient toujours séparés par des atomes de gallium. Il n'y a pas de platine solide qui se forme dans ce système. Il est toujours atomiquement dispersé dans le gallium. C'est vraiment cool et c'est ce que nous avons trouvé avec la modélisation, ce qui est très difficile à observer directement par des expériences."
Étonnamment, c'est en fait le gallium qui entraîne la réaction chimique souhaitée, sous l'influence des atomes de platine situés à proximité.
Le Dr Andrew Christofferson, chercheur associé à Exciton Science au RMIT, explique la nouveauté de ces résultats : "Le platine se trouve en fait un peu en dessous de la surface et active les atomes de gallium qui l'entourent. La magie se produit donc sur le gallium sous l'influence du platine.
"Mais sans le platine, elle ne se produit pas. C'est complètement différent de toute autre catalyse que l'on ait pu montrer, à ma connaissance. Et c'est quelque chose qui n'a pu être démontré que par la modélisation."
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.