Le digallène cationique rompt les liaisons fortes
Alternative aux métaux précieux
Annonces
Une équipe de l'université de Fribourg, dirigée par les professeurs Ingo Krossing et Antoine Barthélemy, étudie les processus chimiques qui pourraient constituer la base de nouveaux systèmes catalytiques plus durables. Dans une étude récente, ils ont démontré qu'un digallène doublement chargé positivement peut activer des liaisons covalentes très fortes. Ce travail a été mis en avant comme "Pick of the Week" dans la revue Chemical Science.
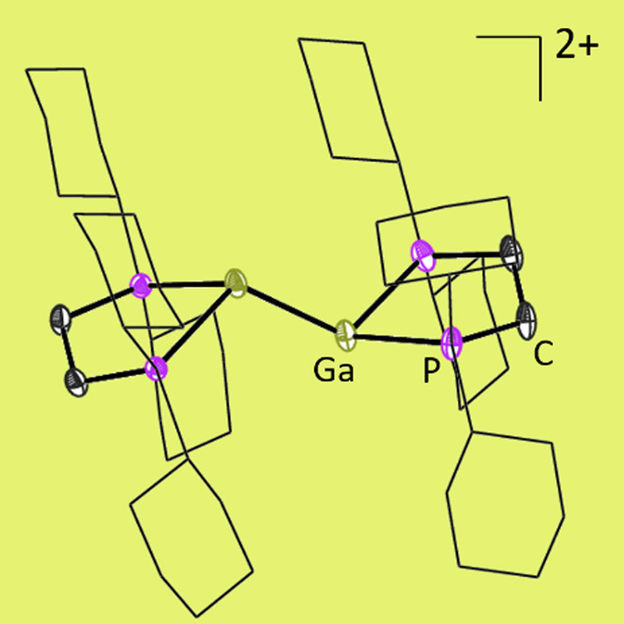
Structure moléculaire du digallène dicationique examiné ici. L'unité réactive de la molécule est la double liaison centrale gallium-gallium.
Antoine Barthélemy / Ingo Krossing
Ingo Krossing, Antoine Barthélemy et leur équipe de l'Institut de chimie inorganique et analytique de l'Université de Fribourg ont étudié la réactivité particulière d'un composé chimique spécifique, un digallène doublement chargé positivement. Ce composé contient deux atomes de gallium et est particulièrement réactif en raison de sa charge doublement positive. Dans leur étude, les chercheurs examinent systématiquement comment des liaisons covalentes normalement très stables peuvent être activées, c'est-à-dire rendues plus réactives, à l'aide d'un tel complexe d'éléments du groupe principal chargé positivement.
L'activation et la conversion des liaisons chimiques impliquent souvent deux étapes : l'addition oxydative, au cours de laquelle un complexe actif entre dans une liaison, et l'élimination réductrice, qui restaure le complexe tout en formant simultanément une nouvelle liaison. Ces étapes sont au cœur de la catalyse redox, c'est-à-dire des systèmes qui ont un effet majeur en petites quantités. Jusqu'à présent, les processus industriels utilisaient principalement des métaux précieux coûteux à cette fin, dont beaucoup sont extraits dans des conditions problématiques. Bien qu'il ait été démontré ces dernières années que les espèces du groupe principal riches en électrons peuvent également s'ajouter aux liaisons par oxydation, ces complexes sont souvent coûteux à produire.
L'équipe de Fribourg a maintenant montré qu'un digallène divalent des groupes principaux peut accomplir cette tâche et activer les liaisons simples fortes H-C, H-N, H-O et les liaisons multiples C≡C/C=C par addition oxydative. Nombre de ces réactions sont décrites pour la première fois pour un composé cationique subvalent du groupe 13. "Le grand avantage pratique du système est que le digallène peut être produit facilement et directement dans la solution de réaction", explique Barthélemy.
La grande réactivité du digallène repose sur deux facteurs : un ligand bisphosphane bidentate riche en électrons, disponible dans le commerce, qui augmente la réactivité du cation, et un anion aluminate faiblement coordinant, qui empêche les interactions indésirables. Des études mécanistiques montrent que l'activation de liaisons multiples se fait de manière coopérative par l'intermédiaire de deux atomes de gallium et permet également l'isomérisation catalytique des oléfines. Dans le cas des liaisons simples, un conformère asymétrique du digallène joue apparemment un rôle important et favorise le mécanisme coopératif. "Ces résultats constituent une étape prometteuse vers une véritable catalyse redox avec des éléments du groupe principal, ce qui serait également très intéressant pour l'industrie chimique", explique M. Krossing. "Ils ouvrent des perspectives pour de nouveaux systèmes catalytiques facilement accessibles avec une réactivité élevée mais contrôlable, non seulement au sein du groupe 13, mais aussi au-delà."
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.














































